|
||||||||
|
近日,我校太阳成集团tyc33455cc分子识别与生物传感研究中心李根喜教授团队在国际著名学术期刊《Journal of the American Chemical Society》上以内封面论文的形式发表了题为“Molecular Characterization of Exosomes for Subtype-Based Diagnosis of Breast Cancer”的原创性研究论文。
乳腺癌是全球女性发病率、死亡率最高的恶性肿瘤,也是我国最值得关注的重大公共卫生问题之一。乳腺癌具有高度异质性,因此,在临床上,精准分辨乳腺癌的亚型特征对乳腺癌患者的个性化治疗和生存率提高至关重要。
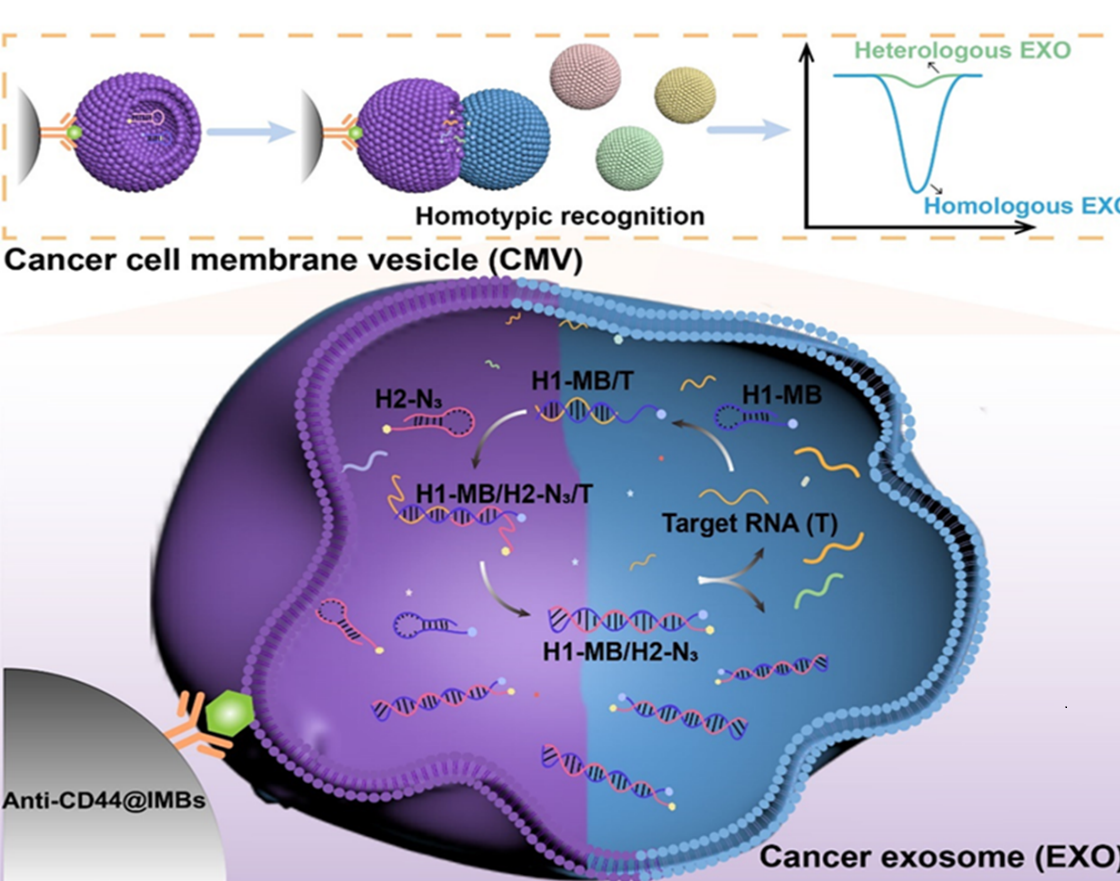
图1基于乳腺癌细胞膜囊泡和外泌体同型识别的乳腺癌亚型分析和诊断新方法示意图 为了更加全面地描述乳腺肿瘤的亚型特征,我校生科院李根喜、赵婧教授与南京医科大学附属江苏省人民医院殷咏梅教授合作,以富含原生肿瘤抗原的乳腺癌细胞膜囊泡为同型识别元件,通过靶向性获取乳腺癌外泌体所携带的分子信息,提出了一种适用于乳腺癌亚型分析和诊断的电化学生物传感方法(图1)。在研究工作中,作者团队首先详细探究了乳腺癌细胞膜囊泡和外泌体之间的同型识别融合现象。以雌激素受体阳性的乳腺癌细胞MCF-7和三阴性乳腺癌细胞MDA-MB-231作为代表性的乳腺癌细胞膜囊泡和乳腺癌外泌体的来源,研究团队发现:由乳腺癌细胞膜制备的仿生囊泡能够准确地识别并融合具有相同亚型特征的乳腺癌外泌体;反之,由于表型差异,非同型的乳腺癌细胞膜囊泡和外泌体之间无法发生有效的相互作用。这些结果证实了富含原生肿瘤抗原的乳腺癌细胞膜囊泡可以作为识别元件,选择性地靶向同型乳腺癌外泌体。
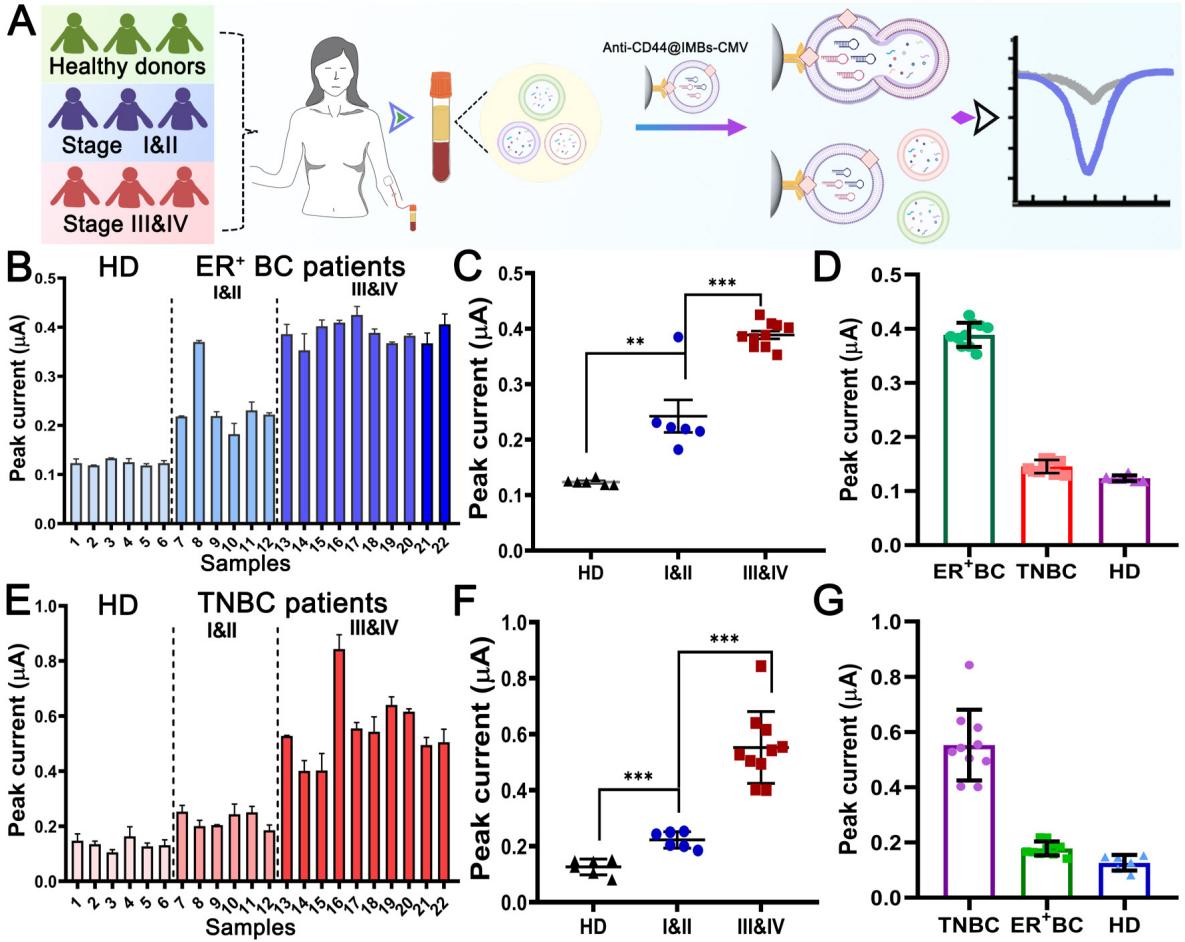
图2乳腺癌细胞膜囊泡和外泌体同型识别驱动的乳腺癌亚型分析和诊断方法的临床应用 以此为基础,作者团队建立了一种以乳腺癌外泌体为分析对象的乳腺癌亚型分析和诊断新方法。该方法一方面借助乳腺癌细胞膜囊泡和外泌体之间的同型识别融合现象,选择性地获取乳腺癌外泌体的亚型特征;另一方面通过膜融合将核酸探针递送至外泌体内部,通过驱动核酸组装反应,测定内源RNA标志物的水平。通过采用具有良好灵敏性的电化学技术为主要信号采集手段,这种将同型识别和内源RNA标志物测定相结合的新方法可以分别实现MCF-7细胞和MDA-MB-231细胞来源外泌体的高选择性和高灵敏性分析。更令人惊喜的是,当被用于临床样本分析时,该方法不仅可以准确识别和测定来自于不同亚型乳腺癌患者样本中的乳腺癌外泌体,为乳腺肿瘤的亚型分析提供信息,而且输出的电化学信号与疾病进展呈明显的正相关性,可满足乳腺癌分期诊断需求(图2)。 上海大学为本论文的第一署名单位,青年教师曹亚和硕士研究生郁晓萌为论文共同第一作者,赵婧教授、殷咏梅教授和李根喜教授为论文共同通讯作者。该研究得到了国家自然科学基金的支持,在此表示感谢。 |
上一条:太阳成集团tyc33455cc李根喜教授团队在《Nucleic Acids Research》发表细菌分析新策略的研究成果
下一条:上海大学青年教师陈雪揭示血小板调控Tfh细胞与机体自身免疫的新功能